Un atom este cea mai mică unitate constitutivă a materiei comune care are proprietățile unui element chimic. Fiecare atom este format dintr-un nucleu și din unul sau mai mulți electroni legați de nucleu. Conform ipotezei De Broglie, atomii sunt suficient de mici încât încercarea de a le prezice comportamentul folosind fizica clasică - de exemplu, ca și cum ar fi niște bile de biliard - dă predicții vizibil incorecte din cauza efectelor cuantice.
Nucleul este format din unul sau mai mulți protoni și, de obicei, dintr-un număr similar de neutroni. Protonii și neutronii se numesc nucleoni. Peste 99,94% din masa unui atom este concentrată în nucleu. Protonii au sarcină electrică pozitivă, electronii au sarcină electrică negativă, iar neutronii nu au sarcină electrică. Dacă numărul de protoni este egal cu cel de electroni, atunci atomul este neutru din punct de vedere electric.
Electronii unui atom sunt atrași de protonii din nucleul atomic de această forță electromagnetică. Protonii și neutronii din nucleu sunt atrași unul de celălalt printr-o altă forță, forța nucleară, care de obicei este mai puternică decât forța electromagnetică de respingere ce acționează între protonii încărcați pozitiv.
Numărul de protoni din nucleu definește elementul chimic căruia îi aparține atomul: de exemplu, toți atomii de cupru conțin 29 de protoni. Numărul de neutroni definește izotopul elementului. Numărul de electroni influențează proprietățile magnetice ale unui atom.
Ideea că materia este alcătuită din unități discrete este o idee foarte veche, care apare în multe culturi antice, cum ar fi Grecia și India. Cuvântul „atom” a fost inventat de vechii filosofi greci. Cu toate acestea, aceste idei își aveau fundamentul mai mult în raționamentele filozofice și teologice, decât în dovezi și experimente. Ca urmare, vederile lor asupra felului cum arată și cum se comportă atomii erau incorecte. Ele nu puteau nici să convingă pe toată lumea, astfel încât atomismul era doar una dintr-o serie de ipoteze concurente cu privire la natura materiei.
La începutul anilor 1800, John Dalton a folosit conceptul de atomi pentru a explica de ce elementele reacționează întotdeauna în raporturi de numere întregi mici (legea proporțiilor multiple). Acest model comun în chimie i-a sugerat lui Dalton că elementele care reacționează în număr întreg multiplu de unități discrete - cu alte cuvinte, atomi. Dalton credea și că teoria atomică ar putea explica de ce apa absoarbe gaze diferite în proporții diferite.
În 1827, botanistul Robert Brown a folosit un microscop pentru a privi granule de praf plutind în apă și a descoperit că ele se mișcau haotic, fenomen care a devenit cunoscut sub numele de „mișcare browniană”. Acest lucru a fost considerat a fi cauzat de faptul că moleculele de apă lovesc granulele.
Fizicianul J. J. Thomson a măsurat masa razelor catodice, arătând că ele sunt formate din particule, dar că acestea sunt de circa 1800 de ori mai ușoare decât cel mai ușor atom, cel de hidrogen. Prin urmare, ei nu erau atomi, ci o nouă particulă, prima particulă subatomică ce a fost descoperită, și pe care el a numit-o inițial „corpuscul”, și mai târziu electron. El a arătat și că ele sunt identice cu particulele emanate de materialele fotoelectrice și de cele radioactive. S-a recunoscut rapid că acestea sunt chiar particulele care transportă curenții electrici în firele de metal, și care poartă sarcina electrică negativă în atomi. Thomson a primit în 1906 Premiul Nobel în Fizică pentru acest lucru. Astfel, el a răsturnat credința că atomii sunt particulele finale, indivizibile, de materie. Thomson a și postulat, incorect, că masa redusă a electronilor încărcați negativ este distribuită prin tot atomul printr-o mare uniformă de sarcini pozitive.
În 1909, Hans Geiger și Ernest Marsden, sub conducerea lui Ernest Rutherford, au bombardat o folie metalică cu particule alfa pentru a observa cum se împrăștie ele. Ei se așteptau ca toate particulele alfa să treacă direct prin folie, cu minime devieri, deoarece modelul lui Thomson spunea că sarcina în cadrul atomului este atât de difuză încât câmpurile lor electrice nu ar putea afecta prea mult particulele alfa. Cu toate acestea, Geiger și Marsden au constatat că unele particule alfa sunt deviate la unghiuri mai mari de 90°, ceea ce în mod normal ar fi trebuit să fie imposibil potrivit modelului Thomson.
În timp ce experimenta cu produsele dezintegrării radioactive, în 1913 radiochimistul Frederick Soddy a descoperit ceea ce părea să fie mai mult decât un singur tip de atom pe fiecare poziție în tabelul periodic. Termenul izotop a fost inventat de către Margaret Todd ca nume potrivit pentru diferiți atomi care aparțin aceluiași element.
Mai târziu în același an, Henry Moseley a furnizat noi dovezi experimentale în favoarea teoriei lui Niels Bohr. Aceste rezultate au rafinat modelul lui Ernest Rutherford și modelul lui Antonius van den Broek, care avansa ideea că atomul conține în nucleu un număr de sarcini nucleare pozitive egal cu numărul (atomic) din tabelul periodic. Până la aceste experimente, numărul atomic nu era cunoscut drept cantitate fizică și experimentală.
Legăturile chimice dintre atomi erau acum explicate, de Gilbert Newton Lewis în 1916, ca interacțiuni între electronii care îi compun. Cum se cunoștea în mare măsură că proprietățile chimice ale elementelor se repetă în conformitate cu o lege periodică, în 1919, chimistul american Irving Langmuir a sugerat că acest lucru ar putea fi explicat prin faptul că electronii dintr-un atom sunt legați sau grupați într-un fel.
Experimentul Stern-Gerlach din 1922 a furnizat dovezi suplimentare ale naturii cuantice a atomului. Atunci când un fascicul de atomi de argint a fost trecut printr-un câmp magnetic de formă specială, fasciculul a fost divizat în funcție de direcția momentului cinetic al atomului, denumit spin. Cum această direcție este aleatoare, era de așteptat ca raza să se răspândească într-o linie.
În 1924, Louis de Broglie a avansat ipoteza că toate particulele se comportă până la un punct ca niște unde. În 1926, Erwin Schrödinger a folosit această idee pentru a dezvolta un model matematic al atomului, care descria electronii ca forme de undă tridimensionale, mai degrabă decât ca particule punctiforme. O consecință a folosirii formelor de undă pentru a descrie particulele a fost că este matematic imposibil să se obțină valori precise atât pentru poziția cât și pentru impulsul unei particule la un moment dat în timp; acest lucru a devenit cunoscut ca principiul incertitudinii, și a fost formulat de Werner Heisenberg în 1926. Acest model a fost în măsură să explice observațiile comportamentului atomic pe care modelele anterioare nu le puteau explica, cum ar fi anumite șabloane structurale și spectrale ale unor atomi mai mari decât hidrogenul.
Dezvoltarea spectrometriei de masă a permis măsurarea cu precizie sporită a masei atomilor. Dispozitivul folosește un magnet pentru a îndoi traiectoria unui fascicul de ioni, și cantitatea de deformare este determinată de raportul între masa unui atom și sarcina sa. Chimistul Francis William Aston a folosit acest instrument pentru a arăta că izotopii au mase diferite. Masa atomică a acestor izotopi variază cu multipli întregi ai unei valori, denumită regula numerelor întregi.
Explicația pentru acești izotopi diferiți aștepta descoperirea neutronului, o particulă fără sarcină, cu o masă similară cu a protonului, de către fizicianul James Chadwick în 1932. În 1938, chimistul German Otto Hahn, un student al lui Rutherford, a direcționat neutronii asupra unor atomi de uraniu pentru a obține elemente transuranice. Experimentele lui chimice au demonstrat, în schimb, producerea de bariu. Un an mai târziu, Lise Meitner și nepotul ei Otto Robert Frisch au confirmat că rezultatul lui Hahn a fost de fapt prima fisiune nucleară experimentală. În 1944, Hahn a primit premiul Nobel pentru Chimie.
În 1950, dezvoltarea unor acceleratoare de particule și detectoare de particule îmbunătățite au permis oamenilor de știință să studieze efectele atomilor în mișcare la energii înalte. Neutronii și protonii s-au dovedit a fi hadroni, adică compuși din particule mai mici numite quarkuri.
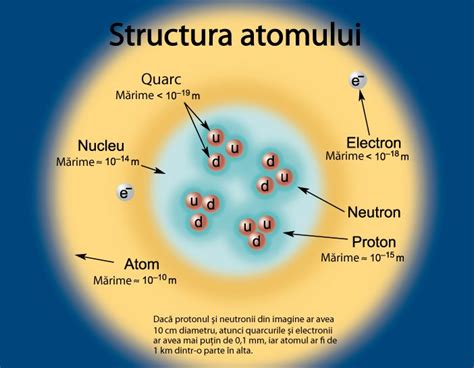
Deși cuvântul atom denumea inițial o particulă care nu poate fi împărțită în particule mai mici, în utilizarea științifică modernă atomul este compus din diferite particule subatomice. Particulele constituente ale unui atom sunt electronii, protonii și neutronii; toate trei sunt fermioni.
Electronul este de departe cel mai puțin masiv din aceste particule, la 9,11×10−31 kg, cu sarcină electrică negativă și cu dimensiune care este prea mică pentru a fi măsurată folosind tehnicile disponibile. Este cea mai ușoară particulă cu masă de repaus pozitivă măsurată. În condiții normale, electronii sunt legați de nucleul încărcat pozitiv prin atracția creată între sarcinile electrice de semn opus. Dacă un atom are mai mulți sau mai puțini electroni decât numărul său atomic, atunci el devine încărcat negativ sau, respectiv, pozitiv în ansamblu; un atom încărcat electric se numeste ion.
Protonii au o sarcină pozitivă și o masă de 1836 de ori mai mare ca a electronului, la 1,6726×10−27 kg. Numărul de protoni dintr-un atom se numește număr atomic. Ernest Rutherford (1919) a observat că azotul, sub bombardament de particule alfa, radiază ceea ce părea a fi nuclee de hidrogen.
Neutronii nu au sarcină electrică și au o masă liberă de 1839 de ori mai mare ca masa electronului, sau 1,6749×10−27 kg, fiind cea mai grea dintre cele trei particule constituente, dar el poate fi redus prin energia de legătură nucleară.
În Modelul Standard al fizicii, electronii sunt cu adevărat particule elementare, fără structură internă. Cu toate acestea, atât protonii cât și neutronii sunt particule compozite alcatuite din particule elementare numite quarkuri. Există două tipuri de quarkuri în atomi, fiecare având o sarcină electrică fracționară. Protonii sunt compuși din două quarkuri up (fiecare cu sarcina +⅔) și un quark down (cu o sarcină de −⅓. Neutronii constau dintr-un quark up și două quarkuri down. Quarkurile sunt ținute împreună de interacțiunea tare (sau forța nucleară tare), care este mediată de gluoni.
Protonii și neutronii, la rândul lor, sunt ținuți unul lângă altul în nucleu de forța nucleară, care este un reziduu al unei forțe tari cu proprietăți oarecum diferite în raport cu raza de acțiune. Toți protonii și neutronii legați din atom formează un mic nucleu atomic, și sunt denumiți colectiv nucleoni. Raza nucleului este aproximativ egală cu 1.07 3√A fm, unde A este numărul total de nucleoni. Acesta este mult mai mic decât raza atomului, care este de ordinul a 105 fm.
Nucleonii sunt legați împreună de un potențial atractiv cu rază mică de acțiune numit forță tare reziduală.
Atomii aceluiași element au același număr de protoni, numit număr atomic. Într-un singur element, numărul de neutroni poate varia, determinând izotopii acelui element. Numărul total de protoni și neutroni determină nuclidul.
Protonul, electronul, neutronul sunt clasificați ca fermioni. Fermionii se supun principiului de excluziune al lui Pauli, care interzice fermionilor identici, cum ar fi mai mulți protoni, să ocupe aceeași stare cuantică în același timp. Astfel, fiecare proton din nucleu trebuie să ocupe o stare cuantică diferită de toți ceilalți protoni, și același lucru este valabil și pentru neutronii din nucleu și pentru toți electronii din norul de electroni.
Pentru atomii cu un număr atomic scăzut, un nucleu care are mai mulți neutroni decât protoni tinde să scadă la o stare de energie mai mică prin dezintegrare radioactivă, astfel încât raportul neutroni-protoni să se apropie de unu. Cu toate acestea, pe măsură ce numărul atomic crește, este necesară o proporție mai mare de neutroni pentru compensarea respingerii reciproce dintre protoni.
Numărul protonilor și neutronilor în nucleul atomic poate fi modificat, de asemenea, deși acest lucru poate necesita energii foarte înalte din cauza forței tari. Fuziunea nucleară apare atunci când mai multe particule atomice se unesc pentru a forma un nucleu mai greu, cum ar fi prin ciocnirea la mare energie a două nuclee. De exemplu, în centrul Soarelui protonii necesită energii de 3-10 keV, pentru a depăși respingerea-bariera Coulomb-și a fuziona într-un singur nucleu.
Fisiunea nucleară este procesul invers, provocarea divizării unui nucleu în două nuclee mai mici-de obicei, prin dezintegrare radioactivă. Nucleul poate fi modificat și prin bombardament cu particule subatomice sau fotoni de mare energie.
Dacă în urma unei reacții de fuziune masa nucleului este mai mică decât suma maselor particulelor separate, atunci diferența dintre aceste două valori pot fi emise sub forma unui tip de energie utilizabilă (cum ar fi o rază gamma, sau energia cinetică a unei particule beta), așa cum descrie formula lui Albert Einstein a echivalenței masă-energie E = mc2, unde m este pierderea de masă și c este viteza luminii. Fuziunea a două nuclee care creează nuclee mai mari cu numere atomice mai mici decât fierul și nichelul-un număr total de nucleoni de aproximativ 60-este de obicei un proces exoterm care eliberează mai multă energie decât este necesară pentru a le aduce împreună. Acest proces de eliberare de energie este cel care face ca fuziunea nucleară din stele să fie o reacție auto-susținută.
Forța nucleară (sau interacțiunea nucleon-nucleon sau forța reziduală tare) este o forță care acționează între protoni și neutronii din atomi. Neutronii și protonii, ambii nucleoni, sunt afectați de forța nucleară aproape identic. Deoarece protonii au sarcină +1 e, ei interacționează printr-o forță electrică care tinde să-i îndepărteze unii de alții, dar la mică distanță forța nucleară de atracție este suficient de puternică pentru a depăși forța electromagnetică. Forța nucleară leagă nucleonii în nucleele atomice.
Forța nucleară este o atracție puternică între nucleoni la distanțe de aproximativ 1 femtometru (fm sau 1,0 × 10 -15 metri), dar scade rapid până la valori nesemnificative la distanțe de peste 2,5 fm. La distanțe mai mici de 0,7 fm, forța nucleară devine una de respingere. Această componentă de respingere este responsabilă de dimensiunea fizică a nucleelor, deoarece nucleonii nu pot ajunge mai aproape unii de alții decât permite forța. Prin comparație, dimensiunea unui atom, măsurată în angstromi (Å , sau 1,0 × 10 -10 m), este cu cinci ordine de mărime mai mare.
Forța nucleară nu este însă simplă, deoarece depinde de spinul nucleonilor, are o componentă tensorială și poate depinde de impulsul relativ al nucleonilor.
Forța nucleară tare este una dintre forțele fundamentale ale naturii. Forța nucleară joacă un rol esențial în stocarea energiei utilizate în energia nucleară și în armele nucleare. Este nevoie de lucru mecanic (energie) pentru a aduce împreună protonii încărcați electric împotriva forței electrice de respingere. Această energie este stocată atunci când protonii și neutronii sunt strânși împreună de forța nucleară pentru a forma un nucleu. Masa unui nucleu este mai mică decât suma totală a masei individuale a protonilor și a neutronilor. Diferența de masă este cunoscută sub denumirea de defect de masă, care poate fi exprimat în echivalent energetic.
Energia se eliberează atunci când un nucleu greu se separă în două sau mai multe nuclee mai ușoare. O descriere cantitativă a forței nucleare se bazează pe ecuații care sunt parțial empirice. Aceste ecuații modelează energiile potențiale internucleonice, sau potențialele. Constantele pentru ecuatii sunt fenomenologice, adică sunt determinate prin adaptarea ecuațiilor la datele experimentale. Potențialele internucleon încearcă să descrie proprietățile interacțiunii nucleon-nucleon.
Descoperirea neutronului în 1932 a arătat că nucleele atomice sunt formate din protoni și neutroni, ținuți împreună de o forță de atracție. Până în 1935, forța nucleară era imaginată ca fiind transmisă prin particule numite mezoni. Această dezvoltare teoretică cuprindea o descriere a potențialului Yukawa, un exemplu timpuriu de potențial nuclear. Mezonii, particule la început pur teoretice, au fost confirmați experimental în 1947. În anii 1970, s-a dezvoltat modelul quarkurilor, în care mezonii și nucleonii erau văzuți ca fiind compuși din quarkuri și gluoni. În timp ce forța nucleară este asociată de obicei cu nucleonii, această forță se resimte, mai general, între hadroni sau particule compuse din quarkuri.
La distanțe scurte (mai puțin de circa 1,7 fm), forța nucleară de atracție este mai puternică decât forța Coulomb de respingere între protoni; ea depășește astfel respingerea reciprocă a protonilor din nucleu. Cu toate acestea, forța Coulomb între protoni are o rază de acțiune mult mai mare, deoarece variază cu pătratul invers al distanței între sarcini, iar respingera Coulomb devine astfel singura forță semnificativă între protoni atunci când distanța între ei depășește aproximativ 2 până la 2,5 fm.
Forța nucleară are o componentă dependentă de spin. Forța este mai puternică pentru particulele cu spinuri aliniate decât pentru cele cu spinuri anti-aliniate. Dacă două particule sunt identice, cum ar fi doi neutroni sau doi protoni, forța nu este suficientă pentru a lega particulele, întrucât vectorii de spin ale celor două particule de același tip trebuie să se îndrepte în direcții opuse atunci când particulele sunt aproape una de alta și sunt (cu excepția spinului) în aceeași stare cuantică. Această cerință impusă fermionilor rezultă din principiul de excluziune al lui Pauli. Pentru fermionii de tipuri diferite, cum ar fi un proton și un neutron, particulele pot să fie apropiate una de cealaltă și să aibă spinurile aliniate fără a încălca principiul de excluziune al lui Pauli și forța nucleară le poate lega (în acest caz, într-un deuteron), deoarece forța nucleară este mult mai puternică pentru particulele cu spinurile aliniate. Dar, dacă spinurile particulelor sunt anti-aliniate, forța nucleară este prea slabă pentru a le lega, chiar dacă acestea sunt de diferite tipuri.
Forța nucleară are și o componentă tensorială care depinde de interacțiunea dintre spinul nucleonului și momentul cinetic al nucleonilor, ducând la deformare față de o formă sferică simplă.
Dezasamblarea nucleului în protoni și neutroni nelegați necesită lucru mecanic împotriva forței nucleare. La fel, se eliberează energie atunci când un nucleu este creat din nucleoni liberi sau alte nuclee: energia nucleară de legătură.
Forța nucleară este aproape independentă de natura nucleonilor, neutroni sau protoni. Această proprietate se numește independență de sarcină. Forța depinde de alinierea spinurilor nucleonilor (dacă sunt paraleli sau antiparaleli), întrucât are o componentă necentrală sau tensorială. Această parte a forței nu conservă momentul cinetic orbital care se conservă sub acțiunea forțelor centrale.
Simetria care rezultă în forța tare, propusă de Werner Heisenberg, este că protonii și neutronii sunt identici în toate privințele, cu excepția sarcinii. Acest lucru nu este complet adevărat, deoarece neutronii sunt puțin mai grei, dar este o simetrie aproximativă. Protonii și neutronii sunt, prin urmare, văzuți ca fiind aceeași particulă, dar cu numere cuantice de izospin diferite; convențional, protonul este izospin în sus, în timp ce neutronul este izospin în jos. Forța tare este invariantă în transformările izospin SU(2), la fel cum alte interacțiuni între particule sunt invariante în transformările de spin intrinsec SU(2). Cu alte cuvinte, atât transformările izospin cât și cele de spin intrinsec sunt izomorfe în raport cu grupul de simetrie SU (2).
Înțelegerea noastră asupra forței nucleare se obține prin experimentele de împrăștiere și din energia de legătură a nucleelor ușoare.
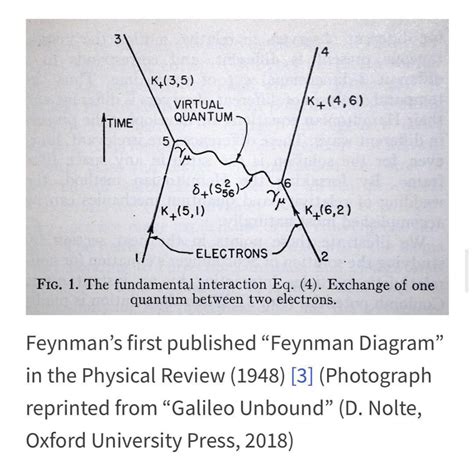
Forța nucleară este un efect rezidual al forței fundamentale tari sau a interacțiunii tari. Interacțiunea tare este forța de atracție care leagă particulele elementare numite „quarkuri” pentru a forma ele însele nucleonii (protoni și neutroni). Această forță mai puternică este mediată de particule numite gluoni. Clasa gluonilor ține împreună quarkurile prin sarcina de culoare, care este analogă sarcinii electrice, dar mult mai puternică. Quarkurile, gluonii și dinamica lor sunt în mare parte limitate la interiorul nucleonilor, dar influențele reziduale se extind puțin dincolo de limitele nucleonului, dând naștere forței nucleare.
Forțele nucleare care apar între nucleoni sunt similare cu forțele din chimie dintre atomii sau moleculele neutre numite forțe London. Astfel de forțe între atomi sunt mult mai slabe decât forțele electrice de atracție care țin atomii înșiși împreună (adică care leagă electronii de nucleu) și raza lor de acțiune între atomi este mai scurtă, deoarece acestea apar dintr-o distribuție ușor eterogenă a sarcinilor din interiorul atomului per ansamblu neutru. În mod similar, chiar dacă nucleonii sunt formați din quarkuri în combinații care anulează majoritatea forțelor gluonice (ei sunt „neutri în raport cu culoarea”), unele combinații de quarkuri și gluoni se fac totuși simțite în exteriorul nucleonilor sub formă de câmpuri de forță nucleară cu rază scurtă de acțiune care se extind de la un n...
Ce se află în interiorul unui atom? Protoni, electroni și neutroni!
tags: #scrieti #sarcina #nucleara #a #atomului #din
