Apoptoza (din limba greacă: αποπτωσις, apo = departe și ptosis = cădere, termen referitor la "căderea frunzelor" toamna) este o formă a morții celulare programate, proces prin care celulele declanșează propria lor auto-distrugere ca răspuns la un anumit semnal.
Apoptoza este o moarte celulară fiziologică, programată genetic, necesară pentru supraviețuirea organismelor pluricelulare, în echilibru constant cu proliferarea celulară.
Termenul a fost propus în 1972 într-un articol publicat în British Journal of Cancer de către John F. Kerr de la Universitatea din Queensland (Australia) împreună cu Andrew H. Wyllie și Alastair R. Currie de la Universitatea din Aberdeen (Scoția), ca rezultat al observațiilor lor făcute în cursul studiilor efectuate asupra țesuturilor cu microscopul electronic.
Fenomenul fusese deja remarcat în 1842 de cercetătorul german Carl Vogt; o descriere mai amănunțită aparține anatomistului englez Walther Flemming (1885).
Apoptoza se deosebește de alte forme de moarte celulară programată, prin faptul că este caracterizată de prezența unui grup de enzime cu activitate proteolitică, așa numitele caspaze, care joacă un rol primordial în procesul de auto-distrugere.
Spre deosebire de necroză, apoptoza reprezintă un proces activ al celulei, este o parte a propriului său metabolism ce comportă consum energetic, se desfășoară ca atare sub un control strict, în așa fel încât să nu producă daune țesutului din jur.
În necroză se observă un fenomen de liză (dezagregare parțială sau totală) celulară, nucleul se distruge până la formarea unei amestec uniform al cromatinei cu citoplasma, membrana plasmatică se distruge rapid, citoplasma se revarsă în afară cu efect dăunător asupra celulelor înconjurătoare. Aceasta provoacă o reacție imunitară a organismului cu răspuns inflamator.
Moartea celulară programată are un rol esențial în dezvoltarea țesuturilor, atât la animale cât și la plante.
Cercetări efectuate asupra embrionului de găină, în special asupra dezvoltării tubului neural, au arătat cum proliferarea selectivă a celulelor combinată cu o apoptoză selectivă determină arhitectonica țesuturilor la animalele vertebrate în timpul dezvoltării.
Astfel, celulele notocordului (coardei dorsale) produc o cantitate de molecule semnalizatoare denumite Sonic hedgehog homolog (Shh), care controlează formarea și diferențierea tubului neural.
La embrionul uman, dispariția apendicelui caudal, din care ar putea crește o coadă ca la alte mamifere, este datorată fenomenului de apoptoză.
Foarte precoce în timpul embriogenezei, creierul trece printr-o primă fază apoptoică care îl remodelează.
Ca răspuns la apariția în organism a unui antigen străin, limfocitele B produc fiecare un anticorp particular, recombinând la întâmplare genele lor codificante de imunoglobuline - recombinări VDJ (variable diversifying joining).
Limfocitele care produc anticorpi inactivi sau autoimuni sunt eliminate prin apoptoză.
În cazul unei infecții virale, limfocitele T citotoxice produc molecule toxice pentru celulele infectate; ele sunt distruse prin apoptoză când infecția este combătută.
Într-un organism adult, numărul de celule conținute de un organ în condiții normale rămâne constant (homeostază).
Elementele figurate din sânge și celulele epiteliale ale țesuturilor de înveliș, de exemplu, sunt în mod permanent reînnoite.
Această proliferare este compensată print-o constantă moarte celulară.
Într-un organism uman mor zilnic cca. 50-70 miliarde de celule datorită proceselor apoptoice.
Homeostaza este menținută când amploarea mitozelor (diviziunilor celulare) dintr-un țesut este în echilibru cu moartea unui număr echivalent de celule.
Celulele mucoasei intestinale sunt într-o reînnoire perpetuă (cu o durată de viață de câteva zile) și migrează din zona profundă a criptelor către vârful vilozităților intestinului subțire, unde asigură funcția de absorbție a substanțelor nutritive.
O celulă normală are în mod permanent nevoie să i se confirme utilitatea ei în organism prin acțiunea factorilor de creștere.
Celula devine sferică și pierde contactul cu celulele din vecinătate.
Există două căi de transducție a semnalelor Fas, depinzând de tipul celulei.
În celulele de tip 1, de ex. timocitele, caspaza-8 activează în mod direct caspaza-3.
În celule de tip 2, ca hepatocitele din ficat, caspaza-8 activează Bid, o proteină pro-apoptoică (BH3 interacting domain death agonist)provocând liberarea citocromului C.
Marea familie a proteinelor aparținând grupului Bcl-2 (B-cell lymphoma 2) joacă un rol major în reglarea apoptozei, în special prin modularea activității anumutor caspaze, mai ales a caspazei-9.
Astfel, împiedicând liberarea de către mitocondrii a citocromului C, Bcl-2 și Bcl-XL inhibă formarea complexelor APAF1/citocrom C/caspază-9 necesar procesului de apoptoză.
Mitocondriile joacă un rol-cheie în reglarea apoptozei.
Într-adevăr, în faza efectoare a apoptozei se deschid porii de tranziție a permeabilității mitocondriilor.
Acești pori sunt canale oligo-proteice constituite la nivelul membranei externe de către VDAC (Voltage Dependent Anion Channel), iar la membrana internă de către ANT (Adenine Nucleotid Translocator).
În urma deschiderii acestor pori se eliberează moleculele pro-apoptoice, ca citocromul C, caspazele 2, 3 și 9 precum și "factorul de inducere a apoptozei" (Apoptosis Inducing Factor - AIF).
AIF este una din moleculele pro-apoptoice liberate de mitocondrii, localizat în spațiul dintre membranele mitocondriale.
Este vorba de o moleculă care posedă o dublă funcțiune: o enzimă, oxidoreductaza, și factorul pro-apoptoic.
Pentru ca această ultimă activitate să devină posibilă, este necesară o redistribuție subcelulară: de la mitocondrie spre metabolismului energetic aerobic și de un stres oxidativ.
Celula pe cale de degradare aflată în ultimul stadiu de apoptoză emite pe membarana citoplasmatică semnale eat me (tradus literal, mâncați-mă), semnale alcătuite din fosfatidilserină.
În mod normal, fosfatidilserina, o fosfogliceridă, se găsește în stratul citosolic al membranei citoplasmatice, însă în timpul apoptozei este redistribuită pe suprafața extracelulară prin intermediul unei proteine ipotetice încă neizolată, denumită în mod arbitrar scramblase (în traducere aproximativă din engleză ca "enzimă care produce dezordine").
Fagocitele necrofage, de ex. macrofagele, au receptori specifici pentru fosfatidilserină.
Eliminarea celulelor moarte este necesară pentru a preveni o reacție imflamatoare.
S-a constatat că factorul de creștere milk fat globule-EGF-factor 8 (MFG-E8) este legat de fosfatidilserina pe membrana celulelor apoptoice și ajută macrofagele în procesul de fagocitare a resturilor celulare.
Macroafgele care conțin corpusculi Fleming (care apar în macrofagele ce au fagocitat alte celule) exprimă într-o manieră forte MFG-E8 pe propria membrană.
Celulele canceroase reprezintă un exemplu de complexe celulare în care mecanismele apoptozei nu mai funcționează.
Anumiți agenți patogeni împiedică inducerea apoptozei, ca de exemplu HHV8 (virusul herpetic responsabil de dezvoltarea sarcomului Kaposi).
În anumite boli neurodegenerative de tipul taupatiilor sunt implicate mecanismele apoptoice, rezultând o supraviețuire a proteinei tau patogenă, care se acumulează în mod anormal, până la moartea celulei nervoase.
Un comportament intempestiv al macrofagelor ar fi implicat și în unele tipuri de reacții exacerbate ale organismului, ca în anumite alergii, în unele boli degenerative sau în anumite reacții la stres (de ex.
Paralel cu maturarea totală a unui organism, se desfășoară și procesul îmbătrânirii, acesta reprezentând inexorabilul declin al capacității de menținere a homeostazei fiziologice.
Îmbătrânirea reprezintă pierderea treptată a masei celulare dintr-un organism, prin apoptoza controlată genetic.
Senescența celulară este un fenomen prin care celulele diploide pierd capacitatea de a se divide.
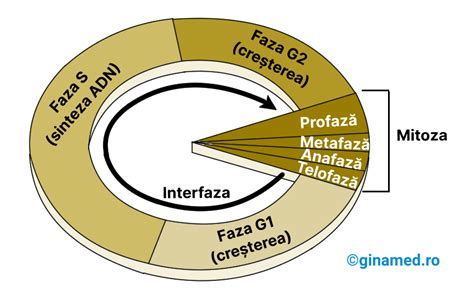
Apoptoza ca fenomen biologic fundamental este o formă specială, programată genetic de moarte fiziologică a celulelor şi constituie o condiţie prealabilă pentru biologia dezvoltării şi reproducerea normală a biodiversităţii viului, în special, pentru funcţionarea sistemului reproductiv şi reglarea spermatogenezei.
Apoptoza joacă un rol important în reglarea spermatogenezei, care începe intensiv în perioada pubertăţii şi continuă pe tot parcursul vieţii organismului.
Rolul apoptozei în reglarea spermatogenezei este bine definit, realizând controlul determinat al numărului de celule germinale şi eliminarea gameţilor patologici, iar rolul apoptozei în dereglarea fertilităţii ejaculatului încă nu este elucidat.
Rolul biologic al mecanismelor de apoptoză în spermatogeneză este de a menţine un număr constant de celule reproductive în sistemul spermatogen, de a asigura raportul optim dintre celule nou formate de diverse tipuri şi de a elimina celulele spermatogene defecte genetic.
Modificările procesului de apoptoză ale spermatozoizilor pot rezulta dintr-un proces iniţiat în timpul spermatogenezei şi din cauza tulburărilor genetice.
Prin urmare, o dereglare a segregării cromozomilor, fixată la nivelul punctelor de reconciliere ale ciclului celular, poate provoca trecerea evoluţiei la fenomenele apoptozei.
Astfel, în baza sintezei informaţiei existente, este posibil de concluzionat că rolul biologic al apoptozei în reglarea derulării spermatogenezei este imens şi inevitabil pentru păstrarea biodiversităţii, însă până în prezent, nu sunt elucidate complet schemele de realizare a apoptozei spermatozoizilor şi procesul de iniţiere a markerilor apoptozei.
Lucrare interdisciplinară cu conţinut ştiinţific pe probleme de biologie, sănătate, dietă şi psihologie, redactată sub formă de naraţiune cu nuanţe umoristice, în anumite capitole, care dezvăluie evoluţia personalităţii autorului, de la primii ani ai vi¬¬¬eţii, până în prezent, confruntarea cu boala şi suferinţele, urmată de prezentarea, cu detalii vii, a teoriei biotransformărilor, etapele de vindecare şi exemple concrete culese de la alte persoane care au reuşit să dobândească aceleaşi aptitudini, prin simpla lectură a publicaţiilor anterioare ale autorului.
Aceasta este o ediţie reactualizată a celor 20 ani de biotransformări (3 februarie 2006 - 3 februarie 2026) în care autorul ne dezvăluie în două volume, (totalizând 546 de pagini) toate experienţele sale, adăugând cel puţin 250 de pagini noi, cu informaţii recente, redactate şi revizuite.
Nu în ultimul rând, autorul îşi dezvăluie preocupările tehnice şi artistice care au contribuit la biotransformarea sa.
Sunt incluse şi CV-ul autorului, precum şi câteva citate şi motto-uri din literatura ce a stat la baza căutărilor sale.
Autorul doreşte să reformuleze şi să îmbunătăţească toate teoriile ştiinţifice conectate direct sau indirect cu experienţa sa de biotransformare, prezentând într-o altă interpretare şi/sau adăugire, o parte din conţinutul publicaţiei sale anterioare „Biotransformări celulare şi fiziologice complexe”.
La toate acestea, autorul a completat cartea anterioară, cu paragrafe si capitole noi, îmbunătăţite, adăugite şi reverificate.
Apoptoza, adesea denumită moarte celulară programată, este un proces natural și foarte reglementat care are loc la toate animalele.
Joacă un rol crucial în diferite funcții biologice, inclusiv dezvoltarea, homeostazia țesuturilor și eliminarea celulelor deteriorate sau inutile.
Se caracterizează printr-o serie de evenimente celulare bine orchestrate care duc la distrugerea ordonată și controlată a unei celule.
Blebbing: Membrana celulei formează proeminențe caracteristice cunoscute sub numele de blebs.
Apoptoza apare din diverse motive, iar reglarea acesteia este esențială pentru menținerea unei funcții celulare adecvate și a sănătății generale.
Procese de dezvoltare: Apoptoza este un mecanism fundamental în timpul dezvoltării embrionare.
Ajută la modelarea și rafinarea țesuturilor și organelor prin eliminarea populațiilor de celule specifice.
Homeostazia tisulară: La organismele adulte, apoptoza contribuie la menținerea homeostaziei tisulare prin echilibrarea proliferării celulare și a morții celulare.
Reglarea sistemului imunitar: Apoptoza este implicată în reglarea sistemului imunitar.
Ajută la eliminarea celulelor imune care nu mai sunt necesare sau care pot fi dăunătoare.
Daune genetice: Celulele cu leziuni genetice severe care nu pot fi reparate pot suferi apoptoză ca mecanism de protecție pentru a preveni propagarea materialului genetic deteriorat.
Apoptoza indusă de hormoni: Hormonii pot declanșa apoptoza în anumite celule.
Acest articol a fost scris de medici pentru a vă ajuta să citiți și să înțelegeți raportul dumneavoastră de patologie.
Contactează-ne dacă aveți întrebări despre acest articol sau raportul dumneavoastră de patologie.
Moartea celulară, la care mitocondriile joacă un rol esențial, este un proces foarte bine reglementat, o desfășurare defectuoasă a sa fiind un factor favorizant pentru o serie de boli degenerative.
Într-un nou studiu, oamenii de știință de la Universitatea din Groningen au prezentat noi informații despre modul în care mitocondriile primesc semnalul de autodistrugere, ce determină apoptoza.
Cum se auto-distruge o celulă? Detaliile acestui proces sunt încă neclare.
Patrick van der Wel, profesor asociat la Universitatea din Groningen, împreună cu omologi de la Universitatea din Pittsburgh au descoperit noi amănunte cu privire la modul în care se inițiază moartea celulară la nivel molecular.
„Membranele mitocondriilor joacă un rol cheie”, explică el.
Cardiolipina, un tip special de lipide membranare, acționează ca un semnal important.
„Dacă este remaniat în interiorul membranei și oxidat, acest lucru poate declanșa moartea celulelor."
Un alt factor este citocromul proteic c, care joacă un rol important în producerea de energie de către mitocondrii, dar care se poate lega și de cardiolipină.
„Credem că poate controla oxidarea cardiolipinei, care face parte din procesul de inițiere a morții celulare programate”, explică Van der Wel.
„În noul nostru studiu, am analizat și mai detaliat interacțiunea dintre citocromul c și membrana mitocondrială”, spune Van der Wel.
Am folosit RMN în stare solidă pentru a detecta poziția și starea tuturor celor 105 aminoacizi din proteină.
Semnalele RMN a doi atomi de carbon conectați într-un aminoacid depind de modul în care interacționează cu alți atomi din moleculă.
Prin urmare, spectrul măsurat al atomilor de carbon poate arăta în ce aminoacizi se află.
Cu ajutorul tehnicii descrise, un aminoacid este vizibil doar într-o parte fixă a structurii proteinei.
Dacă se află într-o parte desfășurată, se poate mișca mai liber și devine invizibil.
Astfel, spectroscopia RMN în stare solidă poate arăta ce părți ale proteinei se mișcă liber și care nu.
Studiul actual oferă o perspectivă fundamentală asupra modului în care moartea celulară programată este reglementată la nivel molecular.
Rezultatele studiului se adaugă la ideea anterioară că oxidarea cardiolipinei de către citocromul c este un proces foarte bine controlat, specific.
Mai mult, știind ce părți ale proteinei se desfășoară, înseamnă că va fi posibil să se dezvolte medicamente care să le stabilizeze sau să le destabilizeze.
Corpurile apoptotice sunt rezultatul unui proces natural numit apoptoză, în care celulele se descompun sistematic și mor ca parte a funcționării normale a organismului.
Apoptoza este un proces extrem de reglementat care implică o serie de evenimente biochimice care conduc la modificări caracteristice ale celulei și la moarte.
În timpul apoptozei, componentele celulei sunt condensate și împachetate în corpuri apoptotice.
Studiul corpurilor apoptotice este important în înțelegerea bolilor în care apoptoza este dereglementată.
În cancer, de exemplu, eșecul celulelor de a suferi apoptoză poate duce la creșterea necontrolată a celulelor.
Deși corpurile apoptotice în sine nu sunt tratate, înțelegerea formării și eliminării lor este vitală pentru dezvoltarea de tratamente pentru bolile legate de apoptoză.
Pacienții care doresc mai multe informații despre apoptoză și implicațiile acesteia pot consulta resurse de la organizații medicale și instituții de cercetare de renume.
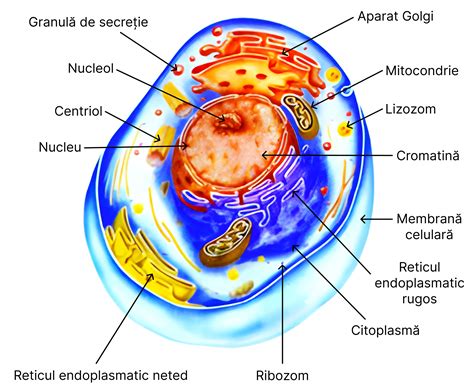
Căile apoptotice
tags: #apoptoza #esuata #la #spermatogeneza
