Restricția de creștere intrauterină (RCIU) reprezintă o complicație frecventă a sarcinii și este una dintre principalele cauze de natimortale, mortalitate neonatală și morbiditate neonatală pe termen scurt și lung la nivel mondial. RCIU afectează dezvoltarea pulmonară, ducând la o morbiditate respiratorie crescută, precum și la o durată crescută de ventilație mecanică la nou-născuții prematuri.
Prin urmare, restricția de creștere intrauterină crește riscul atât al sindromului de detresă respiratorie, caracterizat prin insuficiență respiratorie progresivă imediat după naștere, cât și al displaziei bronhopulmonare (DBP), asociată cu boală pulmonară cronică la vârsta adultă. Un alt rezultat nefavorabil pentru care sugarii cu RCIU prezintă un risc crescut este hemoragia intraventriculară.
RCIU este clasificată în general, în funcție de vârsta gestațională la momentul diagnosticului, în RCIU cu debut precoce (<32 săptămâni) și RCIU cu debut tardiv (≥32 săptămâni). Diferențele dintre aceste două fenotipuri de RCIU în ceea ce privește severitatea, istoricul natural, descoperirile Doppler, asocierea cu complicații hipertensive, descoperirile placentare și managementul constituie baza acestei clasificări.
RCIU cu debut precoce are o prevalență de 0,5%-1%, este de obicei mai severă și este mai probabil să fie asociată cu Doppler anormal al arterei ombilicale decât RCIU cu debut tardiv. Patologia placentară subiacentă este frecvent similară cu cea observată în preeclampsia cu debut precoce (malperfuzie vasculară maternă), ceea ce explică asocierea puternică a RCIU cu debut precoce cu preeclampsia. RCIU cu debut precoce este de obicei mai ușor de detectat în comparație cu RCIU cu debut tardiv, iar istoricul natural tinde să urmeze o secvență predictibilă de modificări Doppler în artera ombilicală și ductus venosus.
Prin urmare, spre deosebire de RCIU cu debut tardiv, unde problema principală este diagnosticul, principala provocare în RCIU cu debut precoce este managementul (momentul nașterii), încercând să se determine echilibrul optim între riscurile opuse de natimortalitate și prematuritate. Acest studiu își propune să stabilească probabilitatea complicațiilor neonatale în funcție de momentul nașterii la feții cu RCIU cu debut precoce pe baza parametrilor Doppler, luând în considerare faptul că în RCIU cu debut precoce, momentul nașterii este ales în principal pe baza parametrilor Doppler, cântărind riscurile și beneficiile pentru sugar.
Materiale și Metode
Un studiu caz-control a inclus 205 gravide cu RCIU cu debut precoce, diagnosticate la Clinica de Obstetrică a Spitalului Clinic de Urgență Municipal din Timișoara, România, între 2018 și 2022. Participantele au fost împărțite în două grupuri (cazuri și control) conform momentului nașterii determinat de parametrii Doppler.
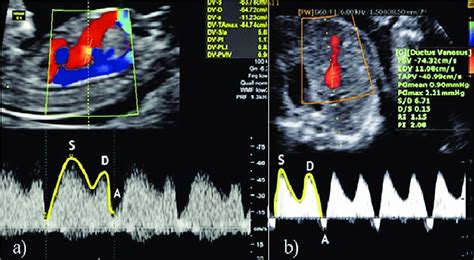
Grupul caz a inclus nou-născuții care au fost născuți la apariția fluxului absent/inversat în diastolă în arterele ombilicale (AO), iar grupul de control a inclus sugarii născuți la apariția undei A inversate/absente în ductus venosus (DV). Nou-născuții au fost urmăriți până la externarea din spital pentru monitorizarea apariției complicațiilor precoce.
Criteriile de includere pentru RCIU cu debut precoce au fost: greutatea fetală estimată (GFE) < percentila a 3-a; vârsta gestațională mai mică de 32 de săptămâni la momentul diagnosticului; și evaluarea Doppler anormală a arterelor ombilicale (AO), arterei cerebrale medii (ACM) sau ductus venosus (DV). Toți sugarii incluși au fost născuți pe baza parametrilor Doppler.
Cazurile care au îndeplinit indicațiile absolute de naștere la momentul diagnosticului au fost excluse: starea maternă (preeclampsie severă, eclampsie, sindrom HELLP), decelerări repetitive ale frecvenței cardiace fetale (FCF), traseu sinusoidal, lipsa variabilității FCF cu decelerări tardive, scorul profilului biofizic (BPF) < 4. Cazurile cu aceste patologii au fost excluse deoarece au necesitat naștere imediată, independent de parametrii Doppler.
Datele au fost extrase din fișele medicale electronice ale pacienților. Diagnosticul a fost stabilit, iar toate ecografiile în timpul sarcinii și studiile Doppler au fost efectuate de un medic specialist în medicina materno-fetală. Vârsta gestațională a fost stabilită prin ecografie de trimestru I. Greutățile fetale estimate și percentilele au fost calculate utilizând formula Hadlock. Măsurătorile Doppler au fost obținute din arterele ombilicale (AO) și ductus venosus (DV) în conformitate cu standardele uniforme.
CTGs anormale au fost caracterizate prin linii de bază FCF fixe, pierderea variabilității FCF, absența accelerațiilor și prezența decelerărilor. Un scor de profil biofizic < 6 a fost considerat anormal. Toate participantele au fost născute prin cezariană.
Rezultatele primare de interes au fost complicațiile precoce la sugarii cu RCIU cu debut precoce. Doi specialiști în neonatologie au stabilit diagnosticul de complicații fetale. Hemoragia intraventriculară (HIV) a fost diagnosticată prin ultrasonografie craniană. Leziunile de HIV au fost clasificate în gradele I-IV. Diagnosticul de DBP a fost stabilit conform atelierului National Institute of Child Health and Human Development (NICHD). Diagnosticul de enterocolită necrozantă a fost stabilit pe baza unei serii de radiografii abdominale.
Calculele statistice au fost efectuate utilizând R version 4.2.0. Variabilele continue au fost prezentate ca mediană (interval interquartilic) și comparate prin testul Mann-Whitney. Variabilele categorice au fost exprimate în număr și procentaj și comparate utilizând testul exact Fisher. A fost efectuată o regresie logistică binomială pentru a evalua valoarea predictivă independentă a momentului nașterii în apariția complicațiilor neonatale precoce.
Rezultate
Un total de 205 gravide cu RCIU cu debut precoce au fost incluse în acest studiu. Vârsta medie a fost de 29,48 ani, fără diferențe statistice între grupul de control și cel de caz. De asemenea, nu au existat diferențe statistice între grupuri în ceea ce privește înălțimea, greutatea, gestația și paritatea. Vârsta gestațională mediană (VG) la diagnostic a fost de 31 de săptămâni de gestație (SG), iar VG mediană la naștere a fost de 32 SG.
Cea mai frecventă anomalie Doppler la feții cu RCIU cu debut precoce a fost fluxul absent în diastolă (FAD) în artera ombilicală, care a fost, de asemenea, semnificativ mai frecventă la cei incluși în grupul caz. În plus, cardiotocografia (CTG) anormală a fost observată semnificativ mai mult la feții incluși în grupul de control.
Rata globală de mortalitate neonatală a fost de 2,0%, fără o diferență statistică semnificativă între cele două grupuri de studiu (p = 0,19). În plus, nu a fost observată nicio diferență semnificativă între ratele de hemoragii intraventriculare (HIV) de gradul I-II în cele două grupuri (p = 0,41). Cu toate acestea, displazia bronhopulmonară și hemoragiile intraventriculare de gradul III-IV au fost găsite mai frecvent la participantele incluse în grupul doi (control).
Vârsta gestațională a fost un factor major în apariția complicațiilor neonatale la sugarii cu RCIU, majoritatea complicațiilor fiind raportate la cei născuți înainte de 30 de săptămâni de gestație. Diferența dintre grupuri a fost momentul nașterii (conform indexilor Doppler) la sugarii cu o vârstă gestațională mai mică de 30 de săptămâni de gestație. La sugarii născuți până la 30 de săptămâni de gestație, hemoragiile intraventriculare de gradul III/IV și displazia bronhopulmonară au fost semnificativ mai frecvente în grupul de control. Dimpotrivă, hemoragiile intraventriculare de gradul I/II au fost mai frecvente la feții a căror naștere a fost amânată până la apariția FAD/fluxului inversat în diastolă (FID) în AO.
Analiza de regresie logistică binomială univariată la feții născuți sub 30 de săptămâni de gestație arată că cei incluși în grupul de control au avut de 30 de ori mai multe șanse să dezvolte displazie bronhopulmonară (p = 0,002) și de 14 ori mai multe șanse să dezvolte HIV gradul III/IV (p < 0,001).
În plus, variabile precum vârsta, CTG anormal și BPP anormal pot fi corelate cu rezultate neonatale nefavorabile. Vârsta gestațională și frecvența BPP-ului anormal au fost similare între cele două grupuri, în timp ce un model de CTG anormal a fost observat mai frecvent la subiecții incluși în grupul de control (3,2% vs. 27,8%; p = 0,02).
Prin urmare, diferențele, în ceea ce privește probabilitatea de a dezvolta HIV gradul III/IV și displazie bronhopulmonară, rămân semnificativ mai mari în grupul de control și atunci când se ajustează pentru vârsta gestațională la naștere. Mai mult, regresia logistică multivariată, incluzând vârsta gestațională, CTG și BPP anormal, arată că displazia bronhopulmonară și hemoragia intraventriculară gradul III/IV sunt de 23 și, respectiv, 70 de ori mai probabile la nou-născuții din grupul de control.
Rezultate la sugarii născuți între 30 și 34 de săptămâni de gestație
Un număr total de 120 de nou-născuți au fost născuți între 30 și 34 de săptămâni de gestație. Dintre aceștia, nu au existat decese neonatale sau sugari care să dezvolte displazie bronhopulmonară și enterocolită necrozantă. În schimb, 31 de nou-născuți au dezvoltat hemoragie intraventriculară, 29 dintre ei de gradul I/II și 2 sugari de gradul III/IV. Hemoragia intraventriculară de gradul I/IV a fost semnificativ mai frecventă la nou-născuții născuți la apariția fluxului absent în diastolă în AO (p < 0,0001). Mai mult, hemoragia intraventriculară de gradul III/IV a apărut doar la nou-născuții incluși în grupul de control (născuți după apariția fluxului inversat în diastolă în AO) (Tabelul 9).
Regresia logistică univariată a arătat că probabilitatea de a dezvolta hemoragie intraventriculară de gradul I/II a fost de 7,76 ori mai mare la nou-născuții a căror naștere a fost amânată până la apariția FID în AO, comparativ cu cei născuți la momentul apariției FAD în AO (Tabelul 10).
Mai mult, regresia logistică multivariată a arătat un risc de 14 ori mai mare de a dezvolta HIV gradul I/II la sugarii incluși în grupul de control, ajustat pentru vârsta gestațională (Tabelul 11).
Discuție
Într-o cohortă de sarcini complicate de RCIU cu debut precoce, s-a observat că complicațiile neonatale precoce au fost asociate cu momentul nașterii în raport cu parametrii Doppler. Sugarii sub 30 de săptămâni au fost examinați separat datorită faptului că, în grupul de control, nașterea a fost decisă conform parametrilor Doppler ai ductus venosus.
În mod tipic, Doppler-ul arterei ombilicale nu este inclus în protocoalele de management pentru RCIU cu debut precoce, până la 30-32 de săptămâni de gestație. În schimb, clinicianul se bazează pe alți indicatori ai sănătății fetale, cum ar fi traseul frecvenței cardiace fetale (FCF), profilul biofizic și velocimetria Doppler a ductus venosus.
În contrast, indicele de pulsatilitate al ductus venosus și variația pe termen scurt a frecvenței cardiace fetale sunt cunoscuți ca predictori importanți ai momentului optim al nașterii înainte de 32 de săptămâni de gestație și corelează cu rezultatul fetal la naștere în anumite studii.
În primul rând, la sugarii născuți sub 30 de săptămâni de gestație, la care nașterea a fost amânată până la apariția undei DV absente/inverse, probabilitatea de DBP a fost de 30 de ori mai mare comparativ cu sugarii născuți la momentul FAD/FID în AO. Mai mult, HIV gradul III/IV a fost semnificativ mai frecventă la sugarii a căror naștere a fost amânată până la apariția undei a DV inversate/absente, comparativ cu cei născuți imediat după apariția unei anomalii a fluxului în artera ombilicală. În plus, probabilitatea unui grad crescut de hemoragie intraventriculară a fost de 14 ori mai mare la sugarii la care nașterea a fost amânată până la apariția undei a DV absente/inverse.
În al doilea rând, studiul a evaluat, de asemenea, probabilitatea complicațiilor neonatale la feții peste 30 de săptămâni de gestație, născuți la apariția FAD în AO (grupul caz) comparativ cu cei a căror naștere a fost amânată până la apariția FID în AO (grupul de control). Sugarii a căror naștere a fost amânată până la apariția FID în AO au avut de 7,76 ori mai multe șanse să dezvolte HIV gradul I/II, comparativ cu cei născuți la momentul apariției FAD în AO.
În general, în studiul nostru, mortalitatea neonatală a fost de 4%, în timp ce 4,9% dintre nou-născuți au dezvoltat displazie bronhopulmonară și 39% hemoragie intraventriculară de diferite grade.
Fetal Medicine Foundation - Ductus venosus
Embriologie și Anatomie a Sistemului Venos Fetal
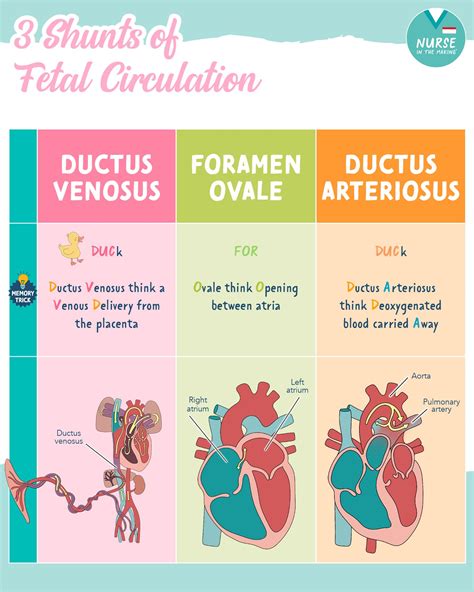
Arhitectura vasculară a ficatului uman se stabilește la sfârșitul săptămânii a 10-a de gestație. Dezvoltarea sistemului circulator fetal este esențială, incluzând structuri precum ductus arteriosus, ductus venosus, foramen ovale și fluxul placentar-ombilical.
Ductus venosus este un șunt vascular care permite sângelui oxigenat din vena ombilicală să ocolească ficatul și să ajungă direct în vena cavă inferioară, protejând fătul de supra-circulația placentară. În timpul trimestrului II și III, fracția de sânge placentar ce trece prin ductus venosus se reduce de la 30% la 20%.
La naștere, acest șunt se închide funcțional (93% dintre sugari la 2 săptămâni), apoi se închide structural și se transformă în ligamentum venosum. Anomaliile includ absența sau persistența ductus venosus.
Sistemul venos fetal se dezvoltă din venele ombilicale, venele viteline și venele cardinale. Vena ombilicală stângă devine calea dominantă pentru sângele de la placentă, direcționându-l prin sinusoidele hepatice. Un canal mare, ductus venosus, se dezvoltă pentru a șunta sângele din vena ombilicală în canalul cardiac drept și apoi în sinus venosus.
Sistemul venos efereent este format din venele hepatice, care transportă sângele din ficat către inimă, iar sistemul aferent include sistemul portal, care livrează sângele de la intestin și placentă la ficat prin vena ombilicală. Vena ombilicală intră în abdomen în ligamentul falciform și se unește cu ficatul pe suprafața sa inferioară, deschizându-se în sinusul portal, care este aliniat cu originea ductus venosus.
Ductus venosus este esențial pentru furnizarea de sânge oxigenat către partea stângă a inimii și pentru dezvoltarea normală a sistemului venos portal intrahepatic. Absența DV poate cauza hemodinamici aberante, cu un efect de "furt" și un flux intrahepatic scăzut, ceea ce poate duce la eșecul transformării venelor viteline în sistemul portal.
| Parametru Doppler pentru Naștere | Complicații Neonatale | Risc Relativ (Interval de Încredere 95%) |
|---|---|---|
| Debutul FAD/FID în AO (Grup Caz) | HIV Grad III/IV | 1 (Referință) |
| DBP | 1 (Referință) | |
| Apariția undei A inverse/absente în DV (Grup Control) | HIV Grad III/IV | 14 (3.2-62.1) |
| DBP | 30 (4.5-201.7) | |
| Debutul FAD în AO (Grup Caz, 30-34 WG) | HIV Grad I/II | 1 (Referință) |
| HIV Grad III/IV | 1 (Referință) | |
| Debutul FID în AO (Grup Control, 30-34 WG) | HIV Grad I/II | 7.76 (1.8-33.1) |
| HIV Grad III/IV | Prezent doar în grupul de control |
tags: #canalul #arterial #ductul #venos #fat #intrauterin
