Infertilitatea este o problemă actuală de sănătate globală, afectând aproximativ 10-15% dintre cuplurile aflate la vârsta reproductivă.
Cauza infertilității este feminina în 40% din cazuri, masculină în 40%, iar în 20% infertilitatea se datorează ambilor parteneri sau are o cauză necunoscută.
Infertilitatea Feminină și Endometrioza
Infertilitatea și endometrioza merg, deseori, în tandem.
În acest sens, una dintre cauzele majore ale infertilității feminine este endometrioza, afecțiune de natură ginecologică cronică și progresivă, caracterizată prin formarea țesutului endometrial în afara cavității uterine.
Endometrioza afectează aproximativ 6-10% dintre femeile care se află la vârsta fertilă și este diagnosticată la 25-50% dintre femeile infertile.
Endometrioza este o afecțiune caracterizată prin prezența țesutului endometrial funcțional (tip glandular și stromal) în afara cavității uterine.
Aceste implanturi ectopice de țesut endometrial se pot localiza pe ovare, trompele uterine, peritoneu, vezica urinară, rect și chiar pe organe care se găsesc în afara cavității pelviene, precum plămânii.
Tocmai din aceste motive, infertilitatea și endometrioza sunt deseori în asociere.
Simptomele endometriozei variază ca severitate, unele paciente putând fi chiar asimptomatice.
Infertilitatea și endometrioza descriu o relație complexă, care implică mecanisme inflamatorii, modificări hormonale, tulburări ovulatorii și chiar afectarea implantării embrionului.
Infertilitatea și endometrioza, după cum deja s-a menționat, deseori merg mână în mână.
Relația dintre acestea este complexă și multifactorială.
Endometrioza moderată/severă poate cauza formarea unor aderențe între ovare, trompele uterine și peritoneu, ceea ce împiedică captarea ovocitului de către trompa uterină și, astfel, fertilizarea acestuia.
Endometriomul ovarian reprezintă o formă de endometrioza chistică.
În jur de 17-44% dintre femeile cu endometrioza au endometriom ovarian.
Infertilitatea și endometrioza pot avea la bază și defecte de implantare a embrionului la nivelul mucoasei uterine.
Pe de altă parte, deși infertilitatea și endometrioza sunt deseori în asociere, există și alternative de tratament care pot îmbunătăți șansele de concepție.
Chirurgia laparoscopică, standardul de aur, poate rezolva infertilitatea și endometrioza mai ales în formele moderate sau severe.
Infertilitatea și endometrioza ușoară nu sunt întotdeauna asociate, dar în unele cazuri, deși este vorba de forma ușoară, boala poate sta în calea obținerii unei sarcini.
Infertilitatea și endometrioza, în cazul în care rezerva ovariană este redusă, poate ridica nevoia fertilizării in vitro (în unele cazuri, chiar cu ovocite donate).
Factori feminini implicați în infertilitate
Tulburări ale procesului de ovulație
Lipsa ovulației în cursul ciclului menstrual poartă numele de anovulație, iar potențialele cauze pot fi:
- Sindromul ovarelor polichistice, condiție care cauzează anovulația sau ovulații neregulate.
- Diminuarea rezervei ovariene ca urmare a declinului natural pe măsură ce femeia înaintează în vârstă, datorită unor afecțiuni congenitale sau a unor condiții medicale sau chirurgicale.
- Amenoreea hipotalamică funcțională determinată de stres, exerciții fizice intense, anorexie.
- Funcția anormală a hipofizei (ex. producerea în exces a prolactinei).
- Insuficiența ovariană prematură, când rezerva ovariană scade înaintea vârstei de 40 de ani. Această condiție poate fi întâlnită și în chimioterapia și radioterapia pelviană.
Alte cauze ale infertilității feminine
- Afectarea trompelor uterine, ca urmare a infecțiilor (de exemplu: Chlamydia) sau a intervențiilor chirurgicale.
- Aderențe la nivelul pelvisului (țesut cicatricial fibros format între organele pelvine) ce se pot constitui în urma infecțiilor, intervențiilor chirurgicale sau endometriozei.
- Afecțiuni ale uterului: malformații uterine, fibroame uterine, polipi, infecții ale endometrului, aderențe la nivelul cavității uterine (sinechii ce pot să apară în urma unui chiuretaj), utilizarea unui dispozitiv intrauterin pentru contracepție (sterilet).
- Afecțiuni ale vaginului sau ale colului uterin: malformații, infecții, cauze imunologice (formarea de anticorpi antispermatici la nivelul glerei cervicale).
Infertilitatea Masculină și Factorii Genetici
Infertilitatea este o problemă majoră de sănătate care afectează 10-15% dintre cupluri, iar în aproximativ jumătate din cazuri poate fi identificat un factor masculin.
Multe cazuri de infertilitate masculină sunt asociate cu oligozoospermie (reducerea producției de spermatozoizi) sau azoospermie (absența spermatozoizilor în ejaculat).
Astfel de alterări în producerea de spermatozoizi pot fi corelate cu modificări histopatologice testiculare de severitate diferită, de la absența completă a celulelor germinale („sindromul existenței doar a celulelor Sertoli” -SCO) la hipospermatogeneză și oprirea maturării.
Pe de altă parte, afectarea spermatogenezei se poate datora mai multor cauze: afecțiuni sistemice, criptorhidie, tulburări endocrinologice, obstrucția/absența căilor seminale, infecții, medicamente, iradiere etc.
Cel puțin la un subgrup din această categorie mare de persoane cu defect de spermatogeneză (~ 30%) este implicată o cauză genetică, ceea ce înseamnă că una sau mai multe gene care influențează spermatogeneza și-au pierdut funcția normală.
Sunt descrise astfel trei cauze genetice de infertilitate masculină:
- anomalii cromozomiale: prezente la 5-10% dintre bărbații cu oligozoospermie și 10-15% dintre cei cu azoospermie; cea mai cunoscută anomalie este sindromul Klinefelter (47, XXY);
- microdeletii ale cromozomului Y: prezente la 10-18% dintre pacienții cu oligo- sau azoospermie severă;
- mutațiile genei fibrozei chistice (CFTR): se transmit autozomal-recesiv; anumite mutații pot determina: absența congenitală bilaterală a canalului deferent (CBAVD), absența unilaterală a acestuia fără manifestări pulmonare sau pancreatice (CUAVD) sau obstrucția canalului deferent; varianta 5T constituie o mutație comună asociată cu CBAVD.
Microdeletiile cromozomului Y constituie o cauză genetică relativ recent descoperită de infertilitate.
Majoritatea acestor anomalii apar de novo și datorită fenotipului asociat cu infertilitate nu sunt de regulă transmise descendenților.
Detectarea microdeletiilor este importantă în special pentru pacienții care intenționează să beneficieze de o reproducere asistată prin ICSI (injecția intracitoplasmatică de spermă) deoarece există riscul ca aceste anomalii genetice să fie transmise și descendenților, ca urmare a suntării mecanismului fiziologic al fertilizării.
Cromozomul Y, unul dintre cei doi gonozomi (cromozomi sexuali), conține 2% din întregul ADN celular și are o lungime de ~60 milioane de perechi de baze.
Are rol distinctiv în determinarea sexului masculin prin gena SRY, alcătuită dintr-un singur exon care codifică un factor de transcripție denumit TDF (testis determining factor).
Mutațiile survenite la nivelul acestei gene dau naștere unui fenotip feminin cu cariotip 46,XY, iar translocația genei SRY pe cromozomul X induce un fenotip masculin cu cariotip 46,XX.
Cei doi cromozomi sexuali X și Y au evoluat dintr-o pereche de cromozomi ancestrali în urmă cu câteva sute de milioane de ani; în timp ce cromozomul X a păstrat multe din proprietățile unui autozom (cromozom non-sexual), cromozomul Y și-a pierdut majoritatea genelor, reducându-și mult dimensiunile.

Astfel, funcția genetică actuală a cromozomului Y este limitată la inducerea dezvoltării masculine în cursul vieții embrionare și la menținerea spermatogenezei la adult.
La cele două capete ale cromozomului Y există regiuni scurte ce sunt identice cu regiunile corespondente de pe cromozomul X, ceea ce indică schimbul de material genetic între aceste zone (recombinare) în cursul meiozei; cele două regiuni pseudoautozomale au fost identificate prin bandare cromozomială și denumite PAR1 și PAR2 (2.6 Mb și, respectiv, 320 kb).
Totuși, mai mult de 95% din materialul genetic al cromozomului Y este specific sexului masculin și nu este implicat în procesul de recombinare X-Y - regiune non-recombinantă (non-recombining region NRY).
În 2003, Skaletsky și colaboratorii săi au secvențiat această regiune și, deoarece au descoperit că la acest nivel se produce un tip special de recombinare genică, au înlocuit denumirea NRY cu regiunea specifică sexului masculin (male specific region of Y, MSY).
MSY constituie de fapt un mozaic de secvențe heterocromatice și eucromatice.
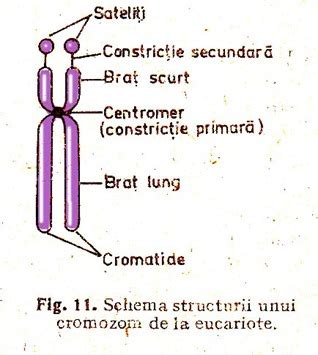
Heterocromatina, considerată inertă din punct de vedere genetic, cu un conținut înalt de secvențe repetitive, este distribuită în principal în porțiunea distală a brațului lung al cromozomului Yq ; mai este întâlnită în zona centromerică, dar și la nivelul unei porțiuni de ~400 kb care întrerupe eucromatina din regiunea proximală Yq.
Eucromatina, acea regiune care conține majoritatea genelor (~23 Mb: 8 Mb pe brațul scurt Yp și ~14.5 Mb pe brațul Yq) este alcătuită din 3 clase de secvențe nucleotidice:
- regiunea X-transpusă (3.4 Mb derivate prin transpoziție din fostele gene X-linkate);
- regiunea X-degenerată (8.6 Mb derivate din autozomul ancestral);
- secvențele ampliconice (10.2 Mb), Y-specifice, caracterizate prin perechi de secvențe aproape identice (99.9% similitudine), organizate în palindroame masive (secvențe care sunt citite la fel pe ambele catene ale ADN-ului dublu elicoidal); fiecare palindrom prezintă două brațe ce pornesc dintr-un punct central, cu o simetrie în oglindă.
Palindroamele MSY, desemnate P1-P8, sunt extrem de mari, cu lungimi ale brațului ce variază între 9 Kb (P7) și 1.45 Mb (P1); ca urmare a structurii lor speciale secvențele ampliconice suferă un proces de recombinare denumit conversie genică - transfer non-reciproc de material genetic între secvențe duplicate din cadrul aceluiași cromozom.
Deoarece regiunea MSY nu participă la crossing-over-ul X-Y din timpul meiozei, aceasta este lipsită de mecanismul de înlocuire a mutațiilor sau a rearanjărilor structurale cu secvențe normale.
Se presupune că fenomenul de conversie genică între secvențele palindromice (recombinarea Y-Y) servește drept mecanism de refacere a secvențelor normale care au devenit nefuncționale pe un braț al palindromului.
Marea majoritate a regiunilor cromozomului Y (57 din 60 Mb) are o rată redusă de recombinare și se transmite în bloc de la o generație la alta.
Markerii cromozomiali cu o rată mutagenă înaltă, cum ar fi regiunile microsatelite, sunt variabile în toate populațiile, iar o combinație specifică de alele poate fi utilizată pentru a defini un haplotip.
Prin utilizarea cromatografiei de lichid sub înaltă presiune denaturantă (DHPLC) au fost depistate 153 haplotipuri la nivelul cromozomului Y uman.
Structura cromozomului Y care se găsește în GenBank aparține haplotipului R1.
Noțiunea de haplotip este importantă deoarece persoanele cu diverse haplotipuri Y pot prezenta fenotipuri diferite (de la normal până la grade variabile de oligozoospermie) atunci când apar microdeletii.
O mare parte dintre genele de pe cromozomul Y au fost identificate relativ recent, fiind clasificate în trei grupuri în funcție de localizare, numărul de copii și modul lor de exprimare:
- a) gene pseudoautozomale, ale căror secvențe sunt identice pe cromozomii X și Y (ca de exemplu ASMTL, MIC2, IL9R) și care sunt exprimate, în marea majoritate a cazurilor, în țesuturi diverse;
- b) gene localizate în regiunile NRY care sunt omoloage cromozomilor X și Y (USP9Y, DBY, UTY); aceste gene sunt exprimate ubiquitar, deși unele dintre ele prezintă produși de transcripție specifici testiculelor;
- c) gene Y-specifice (DAZ, CDY, TSPY); aceste gene sunt prezente în copii multiple, fiind larg distribuite pe cromozomul Y sau grupate într-o regiune mică; sunt exprimate numai la nivelul testiculelor.
O excepție de la această clasificare o constituie gena SRY care determină dezvoltarea testiculelor: deși este Y-specifică, este prezentă într-o singură copie și are un mod diferit de exprimare ce este limitat la creasta genitală, celulele Sertoli (atât la fat cât și la adult) și celulele germinale.
Conform publicației autorilor L. Tiepolo și O. Zuffardi (1976), există o zonă în regiunea MSY care deține un rol important în spermatogeneză, deleția acestei regiuni fiind asociată cu azoospermia și implicit cu infertilitatea; această zonă a fost denumită abreviat AZF (Azoospermia Factor) cu localizare Yq11.23.
Cu toate acestea, complexitatea genetică a locusului AZF a putut fi evidențiată doar în urma dezvoltării tehnicilor STS-PCR (Sequence-Tagged Sites PCR) și de hibridizare Southern Blot care au permis detectarea delețiilor interstițiale submicroscopice (invizibile la nivel citogenetic - microdeletii).
Studiile de mapare moleculară au complicat ipoteza inițială a locusului unic pentru spermatogeneză de pe Yq sugerând existența a 3 regiuni ce pot suferi deleții la bărbații infertili; aceste 3 locusuri au fost denumite AZFa, AZFb și AZFc.
Genele Y din AZFa sunt importante în perioada de embriogeneză și cea pre-pubertară, având rol în diferențierea spermatogoniilor; genele Y din AZFb și AZFc au rol în maturarea deplină a spermatogoniilor până la stadiul de spermatozoizi capabili de fertilizare.
Literatura de specialitate menționează faptul că pacienții cărora le lipsește complet regiunea AZFa nu au celule germinale în epiteliul testicular, diagnosticul clinic fiind „sindromul existenței doar a celulelor Sertoli” (Sertoli-Cell-Only-Syndrome SCO).
Alături de delețiile care apar în una din cele 3 regiuni AZFa, AZFb și AZFc, au fost descrise deleții combinate AZFbc, AZFabc, precum și deleții parțiale AZFc (denumite AZFc/gr/gr).
Frecvența delețiilor, în cazul pacienților cu azoospermie neobstructivă este diferită pentru AZFa, AZFb, AZFc, AZFbc și AZFabc: 4.9%, 15.8%, 59.6%, 13.6% și, respectiv, <1%.
Se presupune că aceste deleții ar surveni în cursul gametogenezei sau în faza timpurie preimplantare și ar implica un deficit al enzimelor responsabile de repararea ADN-ului normal.
Genele din regiunea AZFa
Se estimează că intervalul AZFa se întinde pe o lungime de 792 kb și include două gene funcționale larg exprimate: USP9Y (Y-linked Ubiquitin-Specific peptidase 9) și DDX3Y (DEAD Box polypeptyde 3 Y linked), cunoscută anterior ca DBY.
Rolul exact al genelor din regiunea AZFa nu este încă cunoscut, deoarece mutațiile spontane specifice unei singure gene sunt foarte rar întâlnite.
Deleția completă a regiunii AZFa este relativ rară (frecvență <2% la bărbații cu defect de spermatogeneză) dar bine documentată, fiind întotdeauna asociată cu sindromul SCO.
Gena USP9Y are o lungime de 170 kb, conține cel puțin 46 exoni și codifică o proteină ce funcționează ca o ubiquitin hidrolază C-terminală.
Deși s-a crezut că deleția genei USP9Y este asociată cu azoospermia și oligospermia, un studiu recent a demonstrat că USP9Y nu deține un rol esențial în producerea spermatozoizilor și fertilitate (ar contribui doar la eficientizarea acestor procese).
DDX3Y ar putea reprezenta gena majoră a spermatogenezei în această regiune, este mai frecvent implicată în deleții decât USP9Y, prezentând produși de transcripție specifici țesutului testicular alături de cei ubiquitari.
Gena include 17 exoni și codifică o ARN-helicază ATP dependentă, însă rolul său în dezvoltarea celulelor germinale masculine nu este complet definit.
Genele din regiunea AZFb
Regiunea AZFb cuprinde genele EIF1AY (translation-initiation factor 1A, Y isoform) și RBMY (RNA binding motif on Y).
Rolul genei EIF1AY în spermatogeneză este până acum necunoscut, nefiind raportată nici o deleție specifică a acesteia.
Delețiile parțiale care includ și locusul RBMY, au fost asociate conform studiilor de specialitate cu hipospermatogeneză, iar deleția completă a AZFb este o cauză frecventă de oprire a maturării spermatocitelor, ceea ce sugerează că familia de gene RBMY are un rol important în spermatogeneză, fiind exprimată numai la nivelul țesutului testicular.
Genele din regiunea AZFc
AZFc este regiunea de 3.5 Mb a cărei deleție este cel mai frecvent întâlnită la bărbații cu azoospermie și oligozoospermie; conține mai multe familii de gene implicate în spermatogeneză, candidatul principal în microdeletii fiind DAZ („deleted in azoospermia”);
DAZ are o lungime de 48 kb, este alcătuită din cel puțin 16 exoni și este exprimată specific în țesutul testicular.
Un complex de trei palindroame, cel mai mare având o lungime de 3 Mb și 99.97% identitate între brațele sale cuprinde și regiunea AZFc care suferă frecvent deleție.
Cu o lungime totală de 4.5 Mb, acesta conține șase familii distincte de unități repetitive aproape identice (ampliconi).
Ampliconii b, g, u, r și t au 4, 3, 3, 4 și, respectiv, 2 secvențe repetitive în cadrul haplotipului R1.
Aceste secvențe reprezintă repetiții directe, repetiții inversate și palindroame.
AZFc conține 12 familii de unități de transcripție, toate fiind exprimate în țesutul testicular ca BPY2, DAZ, CDY1, CSPG4LY, GOLGA2LY, TTTY3, TTTY4 etc.
Microdeletiile de la nivelul AZFc pot fi grupate în mai multe subtipuri: deleție completă b2/b4 și deleții parțiale g1/g2, r1/r2 și r2/r4.
Date recente indică faptul că delețiile parțiale AZFc se produc relativ frecvent; în timp ce unele modificări pot avea relevanță clinică contribuția acestora la infertilitatea masculină nu a fost complet analizată.
Factori de Risc pentru Infertilitate
Factori de risc pentru infertilitate la femei
- Vârsta. Odată cu creșterea vârstei scade calitatea și numărul de ovocite, astfel că după vârsta de 35 de ani concepția este mai dificilă și riscul de avort spontan crește.
- Menstruații neregulate sau absente
- Endometrioza
- Avorturile
- Bolile cu transmitere sexuală
- Intervenții chirurgicale în sfera pelvină sau abdominală
- Greutate corporală în exces. Menținerea sau obținerea unei greutăți corporale optime poate să crească șansele de a avea o sarcină.
Factori de risc pentru infertilitate la bărbați
- Consumul de nicotină și alcool
- Bolile cu transmitere sexuală
- Intervenții chirurgicale la nivelul abdomenului sau pelvisului
- Anumite condiții medicale, boli cronice: diabet zaharat, hipertensiune arterială, inclusiv tumori
- Tratamente cu anumite medicamente, inclusiv chimioterapia și radioterapia
- Traumatisme testiculare
- Expunerea la substanțe, la medii toxice
- Temperatura influențează producerea spermei, chiar și câteva grade diferență pot să aibă impact asupra numărului de spermatozoizi care sunt produși.
- Boli genetice cu afectarea fertilității (chiar și în familie, pentru rudele de gradul I)
- Istoric de oreion cu debut după pubertate sau testicul necoborât
- Stresul, depresia severă
Investigații și Opțiuni de Tratament
Cele mai multe cupluri au nevoie de un an pentru a obține o sarcină.
Statistic vorbind, peste 85% din femei rămân însărcinate în decurs de un an.
Fie că este vorba de o fertilitate scăzută, fie că este vorba de infertilitate, sarcina poate fi obținută în cele mai multe cazuri, prin diferite metode de tratament, fertilizarea in vitro fiind doar una dintre ele.
Fertilitatea scade odată cu vârsta, șansele reducându-se începând cu vârsta de 35 de ani.
Contrar opiniei general împărtășite, cauza nu este numai femeia, ci și partenerul bărbat.
Greutatea și stresul pot fi alți doi factori decisivi în ceea ce privește fertilitatea, la fel ca și afecțiunile existente ale partenerilor.
La femei, afecțiunile ginecologice netratate pot duce la infertilitate.
Investigații pentru evaluarea fertilității
Dacă tu și partenerul tău încercați de mai mult de un an de zile să faceți un copil și nu ai rămas însărcinată, cel mai probabil este din cauza unei probleme de fertilitate.
După vârsta de 35 de ani, fertilitatea este mult mai scăzută la ambii parteneri, iar primul pas este să realizezi câteva investigații care să te ajute cu stabilirea următorilor pași pe care este nevoie să îi urmezi atât tu, cât și partenerul tău.
- Profilul hormonal: este o analiză de sânge care măsoară concentrația hormonilor responsabili în obținerea unei sarcini. Acest profil conține analize FSH, LH, TSH, Prolactină, Progesteron, Estradiol, AMH. Probețele pentru aceste analize sunt prelevate în ziua a 2-a sau a treia a ciclului menstrual.
- Histerosalpingografia: Cu ajutorul acesteia sunt evaluate posibilele afecțiuni ale uterului și trompelor uterine, care pot împiedica obținerea unei sarcini. Aceasta se realizează prin injectarea unei substanțe de contrast intrauterin. Dacă trompele uterine sunt înfundate, substanța nu va trece de ele. Medicul de specialitate poate încerca desfundarea lor chiar în timpul procedurii.
- Biopsia endometrială, histeroscopia și laparoscopia sunt alte 3 investigații care au un rol esențial în a verifica funcționarea aparatului reproducător al pacientei.
Soluții moderne pentru infertilitate
În acest articol, vom analiza principalele cauze ale infertilității la ambele sexe, vom explora cei mai importanți factori de risc și vom prezenta opțiunile moderne de tratament disponibile în România, inclusiv cele oferite de rețeaua Wellborn.
Datorită progreselor în medicina reproductivă, există numeroase opțiuni de tratament care pot ajuta cuplurile să-și îndeplinească visul de a deveni părinți.
În cadrul rețelei Wellborn, pacienții beneficiază de tehnici și tratamente moderne, adaptate fiecărui caz în parte.
Tratamente pentru Infertilitatea feminină
- Inducerea ovulației: Cu ajutorul medicației hormonale, medicii pot stimula ovulația, mărind șansele de concepție naturală.
- Inseminarea artificială (IUI): Aceasta implică introducerea spermatozoizilor direct în uter, pentru a facilita fertilizarea. Este recomandată în cazurile de infertilitate inexplicabilă sau ușoare probleme de fertilitate masculină.
- Fertilizarea in vitro (FIV): FIV este una dintre cele mai avansate metode de tratament, prin care ovocitele sunt fertilizate în laborator și apoi transferate în uter. Wellborn utilizează tehnici de embriologie avansate, alături de embriologi și geneticieni cu experiență, pentru a crește șansele de succes.
- Donarea de ovocite și embrioni: În cazurile de rezervă ovariană scăzută sau alte afecțiuni, Wellborn oferă opțiuni de donare de ovocite și embrioni, sprijinind astfel și cazurile complexe.
Tratamente pentru Infertilitatea masculină
- Tehnici de recuperare a spermatozoizilor: În cazurile în care există blocaje anatomice, specialiștii Wellborn utilizează tehnici precum MESA sau TESE pentru recuperarea spermatozoizilor.
- ICSI (injecție intracitoplasmatică a spermatozoizilor): Această tehnică inovatoare este recomandată în cazurile de infertilitate masculină severă și presupune injectarea directă a unui spermatozoid într-un ovul pentru a facilita fertilizarea.
- Crioprezervarea: Spermatozoizii de bună calitate pot fi crioprezervați pentru a fi utilizați în viitor. Wellborn oferă servicii de crioprezervare pentru cuplurile care doresc să își planifice fertilitatea.
Ginecologie - Infertilitatea la femei (cauze și fiziopatologie)
Recomandări pentru determinarea microdeletiilor cromozomului Y
- Evaluarea bărbaților cu azoospermie, oligozoospermie sau infertilitate de cauză neprecizată, pentru stabilirea prognosticului și a opțiunilor terapeutice.
Specimen recoltat - sânge venos.
Recipient de recoltare - vacutainer ce conține EDTA ca anticoagulant.
Cantitate recoltată - 5 mL sânge.
Cauze de respingere a probei - folosirea heparinei ca anticoagulant.
Stabilitate proba - 7 zile la 2-8ºC.
Metoda - analiza prin metoda multiplex PCR a regiunilor AZFa, AZFb, AZFc; prin acest test pot fi detectate >95% din delețiile celor 3 regiuni AZF; sunt folosiți primeri specifici: sY84 și sY86 pentru regiunea AZFa, sY127 și sY134 pentru regiunea AZFb și SY254 și SY255 pentru AZFc.
Interpretarea rezultatelor
Microdeletiile Y pot constitui cauza defectului de spermatogeneză.
Deoarece fertilitatea este compatibilă cu microdeletiile Y (în funcție de statusul fertilității feminine, fertilizarea naturală se poate produce și în prezența unui număr redus de spermatozoizi) este mai adecvat să se considere microdeletiile Y ca fiind cauza oligo-, azoospermiei decât cauza infertilității masculine.
Datele din literatură arată că delețiile Y relevante sunt asociate de obicei cu un număr de spermatozoizi < 1×10^6/mL.
Deleția întregii regiuni AZFa conduce invariabil la sindromul SCO și la imposibilitatea recoltării de spermatozoizi maturi din epiteliul testicular în vederea injecției intracitoplasmatice...
tags: #patologii #ale #meiozei #care #induc #infertilitatea
