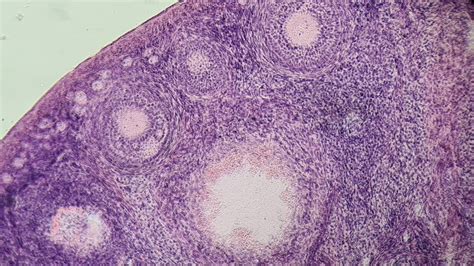
Ovocitele sunt celule sexuale feminine, reprezentând ovule imature care se dezvoltă în interiorul foliculilor ovarieni. În mod obișnuit, un singur ovocit ajunge la maturitate în fiecare ciclu menstrual, proces cunoscut sub numele de ovulație. Acesta, odată eliberat, are potențialul de a fi fertilizat de un spermatozoid, dând naștere unui embrion și, ulterior, unui nou individ.
Ovocitele joacă un rol crucial în ciclul vieții umane, calitatea lor determinând limitele vieții reproductive a femeii, influențând fertilitatea și fiind asociată cu anumuns defecte congenitale majore, cum ar fi sindromul Down.
Femeile se nasc cu un număr finit de ovocite, care scade natural odată cu înaintarea în vârstă. Îmbătrânirea este, de asemenea, principalul factor care contribuie la reducerea calității și stabilității genetice a ovocitelor, explicând dificultățile de concepție după 35 de ani.
Calitatea slabă a ovocitelor este, de obicei, o cauză a infertilității. Deoarece aceasta nu poate fi cuantificată prin teste convenționale, multe cazuri de infertilitate sunt adesea clasificate eronat ca „inexplicabile”.
Anomaliile Cromozomiale și Vârsta
Ovocitul uman este cea mai mare celulă din corp și își menține cromozomii într-o configurație stabilă, dormantă, esențială pentru capacitatea de a forma un embrion sănătos. Calitatea ovocitului reflectă influențele din ultimele nouă luni de dezvoltare. Anomaliile cromozomiale sunt frecvente: la 20 de ani, un sfert din ovocite prezintă astfel de anomalii, iar la 40 de ani, procentul poate ajunge la 40%. De la 35 de ani, aceste defecte genetice cresc exponențial. Un ovocit cu un număr incorect de cromozomi, sau cu cromozomi deteriorați, nu se va dezvolta corect, compromițând viabilitatea unei sarcini.
Cromozomii, pachete de ADN, conțin informațiile genetice necesare dezvoltării organismului. Un ovocit uman conține 23 de cromozomi, jumătatea codului genetic matern, care se combină cu cei 23 de cromozomi paterni din spermatozoid. Majoritatea anomaliilor cromozomiale sunt letale pentru embrionul incipient.
Rata declinului fertilității se accelerează în jurul vârstei de 35 de ani, iar majoritatea femeilor devin infertile până la 45 de ani. Studiile sugerează că și calitatea spermei se deteriorează odată cu vârsta, spermatozoizii bărbaților în vârstă prezentând numeroase mutații ADN.
Factori ce Afectează Fertilitatea
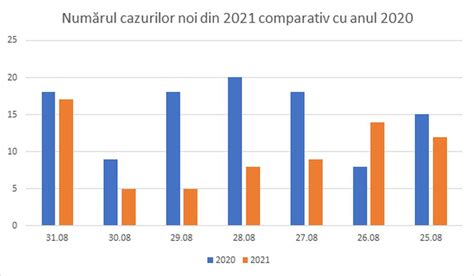
Infertilitatea poate avea un impact semnificativ asupra calității vieții, atât pentru bărbați, cât și pentru femei, generând probleme de sănătate fizică și psihică pe termen lung. Conform unui raport din 2023 al OMS, aproximativ 17,5% din populația adultă se confruntă cu infertilitatea la un moment dat în viață.
Disfuncția țesutului adipos influențează dezvoltarea infertilității prin intermediul adipokinelor, citokine specifice grăsimilor. Funcțiile de reproducere depind de echilibrul energetic, iar anomaliile metabolice pot duce la probleme precum sindromul ovarelor polichistice (SOPC). Femeile obeze întâmpină dificultăți în concepție și sarcină, obezitatea fiind corelată cu o calitate scăzută a ovocitelor și o receptivitate uterină redusă, afectând implantarea.
Exercițiile fizice, în special cele aerobice, pot îmbunătăți nivelul de fertilitate la femeile cu SOPC. Cercetările au evidențiat o legătură între indicele de masă corporală (IMC) și nivelul hormonului Anti-Müllerian (AMH). Un nivel ridicat de acizi grași liberi circulanți dăunează celulelor adipoase, crescând stresul oxidativ și apoptoza celulară, inclusiv la nivelul ovocitelor.
Leptina, secretată predominant de țesutul adipos, joacă un rol în metabolismul hormonilor sexuali. Un nivel crescut de leptină serică la femeile obeze se asociază cu un nivel mai ridicat de leptină în lichidul folicular.
Rolul Hormonilor Gonadotropi
Gonadotropinele reprezintă o clasă de hormoni care stimulează gonadele (ovare și testicule) pentru sinteza și secreția hormonilor sexuali, precum și pentru gametogeneză (formarea ovulelor și spermatozoizilor). Principalii hormoni gonadotropi adenohipofizari cu rol reproductiv sunt hormonul foliculostimulant (FSH) și hormonul luteinizant (LH).
FSH stimulează la femei creșterea și dezvoltarea foliculilor ovarieni, precum și secreția de estrogeni. LH, acționând sinergic cu FSH, contribuie la dezvoltarea corpului galben după ovulație.
La bărbați, LH stimulează secreția de testosteron în testicule, în timp ce FSH este esențial pentru spermatogeneză.
Metabolismul acestor hormoni poate fi influențat de funcția hepatică, disfuncțiile hepatice putând corela cu modificări ale nivelurilor hormonale.
Stimularea Ovariană în Tratamentul Infertilității
Stimularea ovariană reprezintă un pas esențial în majoritatea tratamentelor de fertilitate, inclusiv inseminarea intrauterină și fertilizarea in vitro (FIV). Scopul principal este de a obține un număr mai mare de foliculi maturi într-un singur ciclu menstrual, comparativ cu un singur folicul în ciclul natural, crescând astfel șansele de a obține ovocite mature multiple și, implicit, embrioni de calitate superioară.
Procedura presupune administrarea controlată de medicamente (gonadotropine și/sau alte substanțe) pe parcursul mai multor zile, simulând acțiunea hormonilor naturali responsabili de funcția ovariană. Monitorizarea atentă prin ecografii transvaginale și analize de sânge este crucială pentru a evalua răspunsul ovarian, a ajusta dozele de medicamente și a controla momentul ovulației pentru recoltarea optimă a ovocitelor.
Durata tratamentului de stimulare ovariană variază în funcție de protocolul utilizat și de răspunsul individual al pacientei. Individualizarea tratamentului, adaptat nevoilor specifice ale fiecărei paciente, este esențială pentru maximizarea șanselor de reușită și eficientizarea costurilor.
Eșecul Maturării Ovocitelor (OMA)
Pentru un număr mic de femei, chiar și cu un număr bun de ovule recuperate în urma FIV, sarcina nu se materializează. Această situație frustrantă poate fi cauzată de sindromul Eșecului Maturării Ovocitelor (OMA), în care ovulele se opresc din dezvoltare în mod repetat. Cercetările recente au început să clarifice cauzele și prognosticul acestei afecțiuni.
Un studiu a indicat că, atunci când peste 25% din ovocitele recuperate sunt imature, șansele de a obține o sarcină de succes sunt drastic reduse. În mod obișnuit, un ovocit imatur recuperat ocazional într-un ciclu FIV nu indică o problemă de fond.
O descoperire importantă este că, pentru un subgrup de paciente, cauza OMA este genetică, implicând gene precum PATL2 și TUBB8, care joacă roluri esențiale în etapele de maturare a ovocitului. Totuși, studiile au arătat că mutațiile genetice sunt identificate doar la un procent din pacientele cu OMA. Prognosticul pentru pacientele fără mutații genetice cunoscute poate fi mai favorabil, unele obținând nașteri vii sau chiar concepție naturală.
Maturarea ovocitelor este un proces complex, iar blocajul se poate produce în diferite etape, precum stadiul de Veziculă Germinală (GV) sau stadiul de Metafază I (MI). Blocajul în stadiul GV, mai timpuriu, sugerează o problemă ce uneori poate fi depășită, în timp ce un blocaj în stadiul MI, mai avansat, indică un defect intrinsec mai greu de surmontat.
Distincția între tipurile de blocaj este crucială, demonstrând că nu toate blocajele de maturare sunt similare. O abordare personalizată, combinând testarea genetică cu analiza tipului specific de blocaj, oferă o perspectivă mai clară asupra prognosticului și a opțiunilor de tratament.
Crioconservarea Ovulelor
Crioconservarea ovulelor, sau crioprezervarea ovocitelor mature, reprezintă o metodă de a păstra capacitatea femeii de a avea o sarcină în viitor. Ovulele sunt recoltate, congelate fără a fi fertilizate și stocate pe termen lung.
Când se dorește o sarcină, ovocitul congelat este dezghețat și fertilizat in vitro cu un spermatozoid, iar embrionul rezultat este transferat în uter. Societățile medicale majore consideră crioconservarea ovulelor o opțiune viabilă pentru prezervarea fertilității, în special înainte de tratamente medicale ce pot afecta fertilitatea (chimioterapie, radioterapie) sau în caz de afecțiuni medicale specifice.
Indicații pentru Crioconservare:
- Medicale: Afecțiuni precum anemia falciformă, boli autoimune, tratamente pentru cancer, intervenții chirurgicale ovariene, mutații genetice ce necesită îndepărtarea ovarelor, risc de insuficiență ovariană prematură.
- Elective (sociale): Amânarea maternității din motive personale, având în vedere declinul natural al calității și numărului ovocitelor odată cu înaintarea în vârstă.
Procedura de Crioconservare
Procedura începe cu stimularea ovariană, similară celei din FIV, urmată de recoltarea ovocitelor sub ghidaj ecografic. Ulterior, ovocitele sunt examinate în laborator, evaluate pentru calitate și maturitate, și apoi congelate prin tehnica de vitrificare - un proces ultrarapid care evită formarea cristalelor de gheață și maximizează rata de supraviețuire.
Ovulele congelate pot fi stocate pe termen lung. Utilizarea lor ulterioară implică fertilizarea prin ICSI (Injectare Intracitoplasmatică de Spermatozoizi), urmată de transferul embrionar.
Rata de succes estimată a obținerii unei sarcini pe ovocit congelat variază, iar cercetările continuă pentru a oferi date mai precise.
Fertilizarea In Vitro cu Ovocite Donate
Fertilizarea in vitro cu ovocite donate reprezintă o soluție eficientă pentru femeile care nu pot concepe pe cale naturală din cauza vârstei înaintate, a rezervei ovariene reduse sau a bolilor genetice. De asemenea, este o opțiune pentru pacientele cu menopauză prematură sau pentru cele ale căror ovare au fost afectate de tratamente oncologice.
Succesul procedurii depinde în principal de vârsta donatoarei, optim fiind sub 35 de ani. Procesul implică consultații, evaluări de fertilitate, ecografii, analize de spermă, screening pentru boli infecțioase și găsirea unei donatoare compatibile pe baza unor criterii medicale și personale.
După sincronizarea ciclurilor menstruale, donatoarea trece prin stimulare ovariană, recoltare de ovocite, urmată de fertilizare in vitro în laborator. Embrionii rezultați sunt cultivați și apoi transferați în uterul pacientei. Ulterior, pacienta urmează un tratament hormonal pentru susținerea implantării și face un test de sarcină.
Tabel: Comparație FIV cu Ovule Proprii vs. Ovule Donate
| Aspect | FIV cu Ovule Proprii | FIV cu Ovule Donate |
|---|---|---|
| Sursa ovocitelor | Pacienta | Donatoare |
| Eficiență la vârste înaintate | Scăzută | Ridicata |
| Calitate genetică | Depinde de vârsta și starea pacientei | Asigurată de o donatoare tânără și sănătoasă |
| Costuri | Pot varia, implică stimulare ovariană | Pot fi mai ridicate, includ costurile donatoarei |
| Proces | Stimulare ovariană, recoltare, fertilizare, transfer | Găsirea donatoarei, sincronizare, fertilizare, transfer |
tags: #efectele #hormonilor #gonadotropi #asupra #maturarii #ovocitelor
